不良事件及严重不良事件处理的SOP
Ⅰ. 目的:建立不良事件及严重不良事件处理及报告标准规程,确保受试者的、健康和权益。
Ⅱ. 范围:本规程适用于药物临床试验中不良事件及严重不良事件的处理。
Ⅲ. 规程:
1.定义
1.1不良事件定义
不良事件(Adverse Event, AE)是病人或临床试验的受试者接受一种药物后出现的不良医学事件,但不一定与治疗有因果关系。
1.2严重不良事件定义
SAE指任何剂量的试验药物在观察期间出现的以下不良事件,通常包括:死亡、威胁生命、需住院治疗或延长住院时间、造成终生或明显的残疾/缺陷、先天性异常/生育障碍等。
2.不良事件防范
2.1申办者需提供该药物的临床前性研究资料及其它与性有关的资料,并列入《研究者手册》。
2.2在设计方案中对不良事件应作出明确的定义,并说明不良事件严重程度的判断标准,判断不良事件与试验药物关系的分类标准(如肯定有关、可能有关、可能无关、无关和无法判定)。
2.3在方案中明确设定要求研究者必须如实填写不良事件记录表,记录不良事件的发生时间、严重程度、持续时间、采取的措施和转归。
2.4试验开始前,项目研究小组成员必须熟悉了解该试验用药物已知或未知的副作用与风险,熟悉防范和处理临床试验中受试者损害及突发事件的处理预案的内容。
2.5将研究医生、护士或伦理委员会的联系方式告知患者。
3.不良事件处理
3.1 住院患者
如受试者在住院期间发生不良事件,按以下程序处理:发现受试者出现不良事件后,管床医生或值班医生应及时告知研究者,如有必要,可先对症处理,由研究医师初步评定不良事件的程度分级和与试验药物的相关性,并给予进一步处理意见:
3.1.1 一般不良事件:可密切续观事件的转归或根据试验方案进行相应对症处理;
3.1.2 重要不良事件:研究医师应及时通报主要研究者,并根据方案要求暂停治疗、调整药物剂量并予以针对性处理等处理,如有必要,PI可决定是否紧急揭盲;
3.1.3 严重不良事件:按下述第4点内容及时处理并按相应SOP进行报告。
3.1.4 研究医师根据病情实施处理,如受试者的损害超出研究科室的救治能力时,通知应急小组,启动“防范和处理医疗中受试者损害及突发事件的预案”。
3.2 门诊患者
获知受试者出现不良事件后,研究医师需详细询问受试者当时的症状、体征及所在地点等,对受试者进行必要的解释与开头指导,对不良事件的程度和相关性给予初步评定;
3.2.1 如受试者在当地医疗机构,通过电话与接诊医生取得联系,再次核实不良事件的程度并给予处理意见:
3.2.2 一般不良事件:可赴当地医院初步诊治,并告知密切续观事件的转归;
3.2.3 重要不良事件:建议返院接受诊治或赴当地医院接受诊治,并及时通报主要研究者,如当地医院条件有限,应派出医生前往救治。另携带应急信封以备紧急揭盲用。根据方案要求采用暂停治疗、调整药物剂量和对症治疗等处理。
3.2.4药物临床试验机构办公室协助研究小组追踪不良事件,直到患者得到妥善解决或病情稳定。
4.严重不良事件的处理与报告
4.1考虑为SAE时,由首诊医生通知主要研究者或其他负责医生到场,如病情严重,应一边抢救一边通知项目负责人,如有必要,立即停用试验用药;
4.2 如判断为SAE,则根据临床表现按相关专业临床抢救治疗的规范立即采取相应的治疗或抢救措施;若为药物过量引起的严重毒性,由研究人员决定给予加速药物排泄等抢救措施,尽可能维持病人生命体征的稳定,必要时进行心电监护,如需要可请有关科室会诊、协助处理,启动“防范和处理医疗中受试者损害及突发事件的预案”。
4.3 院外受试者被判断为SAE而又无法前来就诊时,建议受试者及时返院或赴当地医院就诊,同时立即通告项目负责人,获得进一步处理意见;如在当地医院就诊时,与接诊医生取得联系,了解具体情况,予以治疗的建议。必要时携带揭盲信封,前往当地救治或接回本院救治。
4.4 项目负责人确定发生严重不良事件时,必须在24小时内以书面的形式报告:主要研究者,药物临床研究机构伦理委员会、申办单位、药物临床试验机构SAE专员,再由申办者报告至国家食品药品监督管理总局(CFDA),由机构办公室报告至省食品药物监督管理局等。严重不良反应报告的内容可采用申办者提供或CFDA提供的标准表格。申办者报告的部分应保证符合所有法律法规要求的报告规程。(详见SAE报告的SOP)
5 紧急揭盲
发生重要不良事件,在抢救受试者时,需立即查明所用药品的种类由主要研究者决定紧急揭盲。一旦揭盲,该患者将被中止试验,同时将处理结果通知临床监查员。研究人员还应在CRF中详细记录揭盲的理由、日期并签字。
6. 记录
6.1研究医师应做好不良事件的记录,记录至少包括:不良事件的描述,发生时间,终止时间,程度及发作频度,是否需要治疗,如需要,记录给予的治疗。
6.2在原始病历尽可能详细的记录SAE发生、发展、治疗的经过,并记录于CRF表中,对该SAE进行追踪,直到得到妥善解决或病情稳定。明确原因时需向GCP机构的该项目的主要研究者、药物临床研究机构伦理委员会、申办单位、国家食品药物监督管理局等提供较终报告(如必要某些部门应以书面的形式报告)。
7. 不良事件及严重不良事件随访
7.1应对所有不良事件进行追踪调查,直到得到妥善解决或病情稳定,若化验异常应追踪至恢复正常,以确保将受试者损害降至较低。
7.2追踪随访方式可以根据不良事件的轻重选择住院、门诊、家访、通讯等多种形式。
7.3严重不良事件的追踪随访亦应做好相应记录,直至受试者恢复正常。
Ⅳ. 参考依据:《药物临床试验质量管理规范》
Ⅴ. 附注:
1 .不良事件与药物因果关系判断
开始用药时间与可疑不良反应出现时间有无合理的先后关系。
可疑的不良反应是否符合该药物已知的不良反应类型。
所可疑的不良反应是否可以用相关的病理状况、合并用药、现用疗法、曾用疗法来解释。
停药或降低用量,可疑不良反应能否减轻或消失。
再次接触同样药物后是否再次出现同样反应。
因果关系的判断:依据上述五个指标,分析因果关系为肯定、很可能、 可能、可疑和不可能五级。
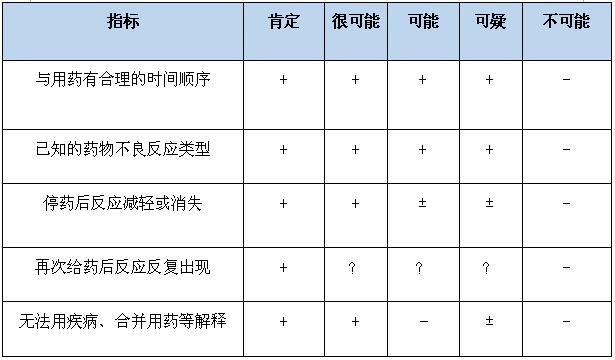
2. CFDA推荐的不良反应分析方法
Ⅱ. 范围:本规程适用于药物临床试验中不良事件及严重不良事件的处理。
Ⅲ. 规程:
1.定义
1.1不良事件定义
不良事件(Adverse Event, AE)是病人或临床试验的受试者接受一种药物后出现的不良医学事件,但不一定与治疗有因果关系。
1.2严重不良事件定义
SAE指任何剂量的试验药物在观察期间出现的以下不良事件,通常包括:死亡、威胁生命、需住院治疗或延长住院时间、造成终生或明显的残疾/缺陷、先天性异常/生育障碍等。
2.不良事件防范
2.1申办者需提供该药物的临床前性研究资料及其它与性有关的资料,并列入《研究者手册》。
2.2在设计方案中对不良事件应作出明确的定义,并说明不良事件严重程度的判断标准,判断不良事件与试验药物关系的分类标准(如肯定有关、可能有关、可能无关、无关和无法判定)。
2.3在方案中明确设定要求研究者必须如实填写不良事件记录表,记录不良事件的发生时间、严重程度、持续时间、采取的措施和转归。
2.4试验开始前,项目研究小组成员必须熟悉了解该试验用药物已知或未知的副作用与风险,熟悉防范和处理临床试验中受试者损害及突发事件的处理预案的内容。
2.5将研究医生、护士或伦理委员会的联系方式告知患者。
3.不良事件处理
3.1 住院患者
如受试者在住院期间发生不良事件,按以下程序处理:发现受试者出现不良事件后,管床医生或值班医生应及时告知研究者,如有必要,可先对症处理,由研究医师初步评定不良事件的程度分级和与试验药物的相关性,并给予进一步处理意见:
3.1.1 一般不良事件:可密切续观事件的转归或根据试验方案进行相应对症处理;
3.1.2 重要不良事件:研究医师应及时通报主要研究者,并根据方案要求暂停治疗、调整药物剂量并予以针对性处理等处理,如有必要,PI可决定是否紧急揭盲;
3.1.3 严重不良事件:按下述第4点内容及时处理并按相应SOP进行报告。
3.1.4 研究医师根据病情实施处理,如受试者的损害超出研究科室的救治能力时,通知应急小组,启动“防范和处理医疗中受试者损害及突发事件的预案”。
3.2 门诊患者
获知受试者出现不良事件后,研究医师需详细询问受试者当时的症状、体征及所在地点等,对受试者进行必要的解释与开头指导,对不良事件的程度和相关性给予初步评定;
3.2.1 如受试者在当地医疗机构,通过电话与接诊医生取得联系,再次核实不良事件的程度并给予处理意见:
3.2.2 一般不良事件:可赴当地医院初步诊治,并告知密切续观事件的转归;
3.2.3 重要不良事件:建议返院接受诊治或赴当地医院接受诊治,并及时通报主要研究者,如当地医院条件有限,应派出医生前往救治。另携带应急信封以备紧急揭盲用。根据方案要求采用暂停治疗、调整药物剂量和对症治疗等处理。
3.2.4药物临床试验机构办公室协助研究小组追踪不良事件,直到患者得到妥善解决或病情稳定。
4.严重不良事件的处理与报告
4.1考虑为SAE时,由首诊医生通知主要研究者或其他负责医生到场,如病情严重,应一边抢救一边通知项目负责人,如有必要,立即停用试验用药;
4.2 如判断为SAE,则根据临床表现按相关专业临床抢救治疗的规范立即采取相应的治疗或抢救措施;若为药物过量引起的严重毒性,由研究人员决定给予加速药物排泄等抢救措施,尽可能维持病人生命体征的稳定,必要时进行心电监护,如需要可请有关科室会诊、协助处理,启动“防范和处理医疗中受试者损害及突发事件的预案”。
4.3 院外受试者被判断为SAE而又无法前来就诊时,建议受试者及时返院或赴当地医院就诊,同时立即通告项目负责人,获得进一步处理意见;如在当地医院就诊时,与接诊医生取得联系,了解具体情况,予以治疗的建议。必要时携带揭盲信封,前往当地救治或接回本院救治。
4.4 项目负责人确定发生严重不良事件时,必须在24小时内以书面的形式报告:主要研究者,药物临床研究机构伦理委员会、申办单位、药物临床试验机构SAE专员,再由申办者报告至国家食品药品监督管理总局(CFDA),由机构办公室报告至省食品药物监督管理局等。严重不良反应报告的内容可采用申办者提供或CFDA提供的标准表格。申办者报告的部分应保证符合所有法律法规要求的报告规程。(详见SAE报告的SOP)
5 紧急揭盲
发生重要不良事件,在抢救受试者时,需立即查明所用药品的种类由主要研究者决定紧急揭盲。一旦揭盲,该患者将被中止试验,同时将处理结果通知临床监查员。研究人员还应在CRF中详细记录揭盲的理由、日期并签字。
6. 记录
6.1研究医师应做好不良事件的记录,记录至少包括:不良事件的描述,发生时间,终止时间,程度及发作频度,是否需要治疗,如需要,记录给予的治疗。
6.2在原始病历尽可能详细的记录SAE发生、发展、治疗的经过,并记录于CRF表中,对该SAE进行追踪,直到得到妥善解决或病情稳定。明确原因时需向GCP机构的该项目的主要研究者、药物临床研究机构伦理委员会、申办单位、国家食品药物监督管理局等提供较终报告(如必要某些部门应以书面的形式报告)。
7. 不良事件及严重不良事件随访
7.1应对所有不良事件进行追踪调查,直到得到妥善解决或病情稳定,若化验异常应追踪至恢复正常,以确保将受试者损害降至较低。
7.2追踪随访方式可以根据不良事件的轻重选择住院、门诊、家访、通讯等多种形式。
7.3严重不良事件的追踪随访亦应做好相应记录,直至受试者恢复正常。
Ⅳ. 参考依据:《药物临床试验质量管理规范》
Ⅴ. 附注:
1 .不良事件与药物因果关系判断
开始用药时间与可疑不良反应出现时间有无合理的先后关系。
可疑的不良反应是否符合该药物已知的不良反应类型。
所可疑的不良反应是否可以用相关的病理状况、合并用药、现用疗法、曾用疗法来解释。
停药或降低用量,可疑不良反应能否减轻或消失。
再次接触同样药物后是否再次出现同样反应。
因果关系的判断:依据上述五个指标,分析因果关系为肯定、很可能、 可能、可疑和不可能五级。
2. CFDA推荐的不良反应分析方法

- 上一篇:没有了
- 下一篇:非注册类临床试验运行管理制度和流程



